Аффиннаж золота и серебра
Аффинажные заводы занимаются переработкой шлихового и самородного золота, которое выделяется в ходе гравитационного обогащения россыпей и руд, золота из амальгам и т.п. Кроме того, здесь происходит переработка производственного и бытового лома, старых монет, сплавов и т.п. материалов.
Во время переработки представляется возможным получение не только золота и серебра, но и платиновых металлов, меди, свинца, сурьмы, олова, висмута и т.п. примесей.
Чаще всего для отражения того, сколько же в сплаве находится благородного металла, используется термин пробы (тысячная доля массы). Лигатура – это общий объем неблагородных примесей.
Таблица 1 - Состав главных видов сырья
|
Материал |
Содержание проб |
|||
|
золото |
серебро |
платиноиды |
лигатура |
|
|
Металл доре из электролитных шламов меди |
20-120 |
830-950 |
До 5 |
30-60 |
|
То же, со свинцовых заводов |
До 40 |
950-990 |
До 0,1 |
10-20 |
|
Лом |
До 1 |
400-850 |
- |
150-600 |
|
Вторичное золото |
950-990 |
10-30 |
- |
10-20 |
Необходимо отметить, что зачастую отдельные партии сырья могут иметь небольшую массу и быть неоднородными. Чтобы усреднить и уточнить расчеты отмечается использование приемной плавки внутри индукционных печей, а также апробация полученных слитков.
Для отделения лигатуры и основной массы серебра, жидкий сплав должен пройти процедуру продувки хлором в графитовых тиглях. Далее осуществляется хлорирование всех металлов, а хлориды преимущественно должны при этом раствориться в шлаке (для его получения пользуются бурой, содой и песком).
Таблица 2 - Изобарные потенциалы образования хлоридов при 1200 °С и температуры их кипения
|
хлорид |
AuCl3 |
PtCl2 |
PdCl2 |
FeCl3 |
AgCl |
CuCl |
PbCl2 |
ZnCl2 |
|
|
0 |
21 |
50,3 |
188,6 |
251,4 |
314,3 |
419 |
686,6 |
|
tкип, °С |
~265 |
- |
- |
315 |
1550 |
1366 |
950 |
732 |
В первую очередь происходит возгонка и переход в шлак хлоридов, состав которых представлен элементами лигатуры, после этого – AgCl, и только после этого – AuCl3. Как только появляются первые признаки, подтверждающие хлорирование золота, процесс продувки прекращается, металл должен быть разлит по изложницам, и передан в валютный фонд. Кроме того, представляется возможным проведение нижеописанной процедуры электролиза, которая позволяет получить более высокое качество очистки. Ее осуществление необходимо для случаев, когда состав материала представлен платиноидами.
Состав хлоридного шлака преимущественно представлен AgCl и CuCl, он подвергается дроблению, после чего грузится в мешки, и располагается в ванной, где находится разбавленная серная кислота и листы железа. При этом ионы Fe2+ используются для восстановления серебра:
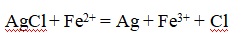
Хлорид меди подвергается окислению:
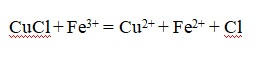
В результате того, что Cu2+ проникается сквозь ткань мешка, осуществляется его цементирование железом. Железо также используется для восстановления ионов Fe3+, поэтому их массовая часть в растворе является очень маленькой, следовательно, происходит сдвижение вправо равновесия реакции, в ходе которой серебро восстанавливается железом. Для того чтобы процедура была завершена в достаточной мере, требуется порядка двух суток, а температуры раствора при этом должна находиться в пределах 90-100 ° C.
Далее осадок цементного серебра подвергается прессовке, плавке и отливке в аноды по 10кг (плиты, толщина которых порядка 10мм). Их состав должен быть представлен не более чем 200 пробами золота и 75 пробами лигатуры.
Процесс электролиза серебра
Роль электролита в данном случае отводится раствору AgNO3, активность которого составляет 1моль/л (до 100 г/л Ag).
После того, как аноды растворяются, раствор пополняется серебром, медью, свинцом, висмутом и иными примесями. Золото выпадает как порошкообразный шлам, состав которого представлен платиновыми металлами, селеном, теллуром, серой и иными примесями, которые не растворяются в электролите.
Для изготовления катодных основ пользуются тонкими алюминиевыми или серебряными листами.
Для катодного осадка серебра характерно наличие рыхлой крупнокристаллической структуры; он может быть легко счищен с катодной основы, и оказаться на дне ванны. Для избегания смешивания осадка чистого серебра с золотым шламом, аноды должны располагаться в тканевых мешках.
Для растворения 10мм анодов требуется порядка суток. После этого происходит возвращение нерастворенного осадка на плавку, из анодных чехлов происходит выгрузка золотого шлама, а извлечение кристаллов чистого серебра со дна ванны осуществляется при помощи алюминиевых дырчатых черпаков.
При этом показатель плотности тока должен находиться в пределах 0,4-0,6 кА/м2, электролит должен быть подвержен энергичному перемешиванию. Недопустимо, чтобы в нем существенно накапливались примеси, в т.ч. медь, превышение массовой доли которой в растворе показателя в 4-5 % может стать причиной загрязнения катодного осадка.
Когда золота будет свыше 200 проб, оно будет приводить к пассивированию анодов, следовательно, начинается процесс выделения кислорода, а также происходит существенный скачок напряжения в ванной.
Для изготовления ванн, емкость которых не превышает 0,6 м3, используется винипласт, а для их укрепления используется каркас из железа или дерева. Выделяемое током тепло используется, чтобы поддерживать комфортную для электролита температуру на уровне 40 градусов. Чтобы перемешивать раствор используется воздух. Состав электролита и плотность тока во многом оказывают влияние на показатель напряжения в ванной.
Чистота осадка серебра, когда им была пройдена промывка при помощи разбавленной азотной кислоты, воды, а также процедура переплавки, составляет 999,9 проб. Использование электролиза дает возможность получения металла с 999,99 или 999,999 пробой.
Отдельные ванные с анодами, представленными низкопробными сплавами, используются для обеднения отработанного электролита серебром.
Электролиз золота
Поступлению металла на электролиз предшествует процедура хлорирования. Кроме того, в данном процессе используются и полученные в ходе электролиза серебра шламы, которые проходят химическую очистку. Все должно быть расплавлено в индукционной печи, и впоследствии отлито в аноды прямоугольной формы, масса каждого из которых составляет 2-3 кг.
Роль электролита отводится раствору НАuСl4 и НСl (до 200 г/л Аu и 80 г/л НСl). Для растворения золота используется реакция:
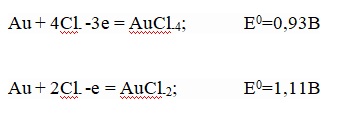
Ионы AuCl-2 могут появляться в результате концентрационной поляризации или в результате того, что на аноде формируется корка AgCl. Но практически сразу происходит процесс их диспропорционации, при котором выделяются выпадающий в шлам осадок металла:
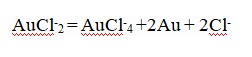
Если кислотность и температура будут недостаточными, то происходит пассивирование золотых анодов, они перестают растворяться, и начинает выделяться хлор

Если кислород перенапрягается на золоте, то он не будет выделяться. Оптимальная температура для осуществления электролиза составляет 50-60 градусов. Кроме того, происходит процесс растворения и накопления в электролите палладия и платины:
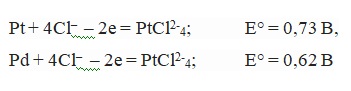
На основании составляющих лигатуры – меди, свинца, висмута, железа, олова, сурьмы и т.п. металлов, происходит формирование простых ионов или же комплексных хлоридов. В большинстве случаев они не приводят к затруднениям при растворении анода. В результате переходящего в раствор в виде Fe2+ железа происходит восстановление золота, в результате чего возрастает его переход в шлам.
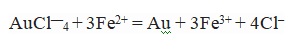
Серебро дает нерастворимый хлорид.
Если сплав представлен менее чем полусотней проб серебра, его хлорид не будет вызывать осложнений. Если же проб больше, то анод покроется коркой из АgCl, которая будет мешать растворению золота.
Способ Вольвиля используется для растворения золотых анодов, состав которых представлен до 200 проб серебра, с использованием ассиметричного тока. Для этого через ванную одновременно должны пропускаться одинаковые по силе переменный и постоянный токи.
Необходимо отметить минимальную вероятность того, что катодный осадок будет загрязнен при помощи примесей. Однако вполне вероятным видится то, что вместе с золотом осядет платина и палладий, особенно, если плотность тока будет высокой. Чтобы избежать этого, в каждом литре раствора должно быть не более 15г палладия и до 50г платины. Других примесей в растворе, содержащем не менее 100 г/л золота, не должно быть больше Сu 90 г/л; Рb 1,5 г/л; Те 4 г/л и 2 % Fe.
Для обеднения отработанного электролита по золоту используются отдельные ванны с анодами из графита, затем для выделения из него золота и платиноидов могут быть использованы самые различные способы.
Для осуществления электролиза золота используются фарфоровые (иногда винипластовые) ванны, емкость которых составляет 25 литров. Аноды должны быть выстроены в ряд и подвешены на штанги из серебра, после чего напротив каждого ряда располагается катод, на котором устанавливается 0,2 мм рифленая золотая фольга. Установка ванн происходит в водяных банях, а для перемешивания электролита используется воздух.
Общий показатель суммарной плотности постоянного и переменного тока может доходить до 1,5 кА/м2, показатель напряжения в ванной находится на уровне 1 В. Механическая очистка при помощи щеток, а также промывка при помощи аммиака и соляной кислоты позволяет добиться чистоты катодного осадка на уровне 999,9 проб.